環保資訊
聯係方式
-
公司:伟德官网地址
聯係人:李先生
電話:18576851991
傳真:0769-28636041
網址:www.chengaa.com
郵箱:1218061775@qq.com
地址:東莞市虎門鎮莞太路271號1棟
與(yu) 幹法脫硫相比,濕法脫硫具有占地麵積小、設備簡單、操作方便、投資少等優(you) 點,因 此脫硫除H2S方法正向著濕法轉變,濕法也是目前常用的方法。按脫硫劑的不同,濕法脫硫 又可以分成液體(ti) 吸收法和吸收氧化法兩(liang) 類。液體(ti) 吸收法中有利用堿性溶液的化學吸收法、利用 有機溶劑的物理吸收法,以及同時利用物理吸收和化學溶劑的物理化學吸收法;而吸收氧化法 則主要采用各種氧化劑、催化劑進行脫硫。這些方法一般均可副產(chan) 硫、硫酸和硫酸釵等。 一般化工、輕工等行業(ye) 排出的含H2S濃度高、總量小的廢氣,常用化學吸收法或物理 吸收法處理;對於(yu) 含H2S濃度較高而且總量也很大的天然氣、煉廠氣,則應以回收硫黃為(wei) 主要技術政策,常用克勞斯法及吸收氧化法處理,而對於(yu) 低濃度H2S氣體(ti) ,一般使用化學 吸收法或吸收氧化法淨化。
(-)液體(ti) 吸收法NF
1-吸收劑的選擇與(yu) 要求
由於(yu) H2S的水溶液中含電離出的[H+],以致影響了淨化過程的化學平衡,當pH值 增加時,溶解度也會(hui) 相應地增加,但作為(wei) 一般規律,吸收能力強的溶劑的再生也是較困難 的,所以目前一般不采用強堿性溶液,而大多采用pH值在9〜11之間的強堿與(yu) 弱酸的鹽 溶液。 為(wei) 了使吸收劑pH值不隨H2S吸收後變化過大而影響操作的穩定性,所選用的吸收劑 應該是緩衝(chong) 溶液。.常用的緩衝(chong) 溶液(吸收劑)為(wei) 強堿弱酸所組成的鹽溶液,如碳酸鹽、硼酸 鹽、磷酸鹽、酚鹽和酚的衍生物、氨基酸等有機鹽以及弱堿溶液,如氨、乙醇胺等。 對用於(yu) 物理吸收法的有機溶劑的要求是有機溶劑對H2S的溶解度應比水高出數倍,而 對■氣流中的主要組分(如氫和燒類)的溶解度較低。此外,還應該有很低的蒸氣壓、低黏度 和低的吸濕性,對普通金屬不蝕,也不會(hui) 與(yu) 氣體(ti) 中其他組分起作用才行。目前國內(nei) 外常用的 有機溶劑有甲醇、N-甲基-27比咯烷酮、碳酸丙烯酯、環丁硯等。 脫硫過程要求吸收劑對S的溶解度大,所以應在低溫高壓下進行吸收。但溫度過低,溶 液黏度增大,流動阻力增加,而且化學反應速度也會(hui) 減慢,反而不利於(yu) 吸收。再生過程中希 望硫的溶解度小,應該在高溫低壓下進行解吸。因此工業(ye) 上一般是在常溫下吸收,而在常溫 或加熱條件下再生;加壓或常壓下吸收,常壓或真空下再生。
2.弱堿溶液的化學吸收法
目前工業(ye) 中廣泛采用的弱堿溶液化學吸收法主要是乙醇胺法。利用乙醇胺易與(yu) 酸性氣體(ti) 反應生成鹽類,在低溫下吸收,在高溫下解吸的性質,可以脫除H?S等酸性氣體(ti) 。常用的 乙醇胺類吸收劑有一乙醇胺(MEA)、二乙醇胺(DEA)等,並分別稱為(wei) MWA法和 DEA 法。 從(cong) 乙醇胺類化合物的結構來看,各種化合物至少都有一個(ge) 輕基和一個(ge) 氨基,一般認為(wei) 輕 基能降低化合物的蒸氣壓並增加在水中的溶解度;而氨基則在水溶液中提供了所需的堿度, 以促使對酸性氣體(ti) 的吸收。例如,一乙醇胺的水溶液吸收H2S的化學反應為(wei) :
2RNH2 + H2S— (RNH3)2S (10-4)
(RNH3)2S+H2S— 2RNH3HS (10-5)
當氣體(ti) 中存在C02時,也同時被吸收:
2RNH2+CO2 + H2O― (RNH3)2CO3 (10-6)
(RNH3)2CO3 +CO2 + H2O —> 2RNH3 HCOs (10-7)
2RNH2+CO2— RNHCOONHsR (10-8)
雖然上述生成物均為(wei) 固定的化合物(有些將分離並結晶出來),但在正常情況下,它們(men) 具有相當大的蒸氣壓,所以平衡溶液的組成隨溶液麵上酸性氣體(ti) 的分壓而變化。由於(yu) 這些生 成物的蒸氣壓隨溫度升高而迅速增加,所以加熱便能使被吸收的氣體(ti) 從(cong) 溶液中蒸出。各種醇 胺吸收H2S流程的基本形式如圖10-4所示。
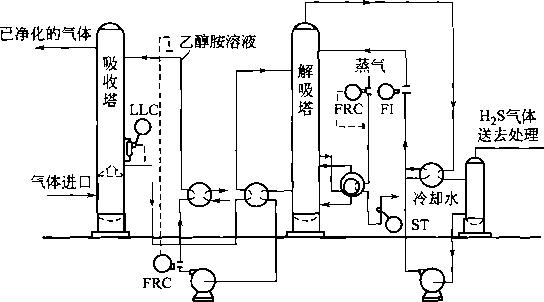
圖10-4用醇胺吸收H2S氣體(ti) 的流程
LLC—液位控製器;FRC-流量記錄控製器;FI—流量指示器;ST—汽水分離器
一乙醇胺溶液(MEA) —般被認為(wei) 是一種對H2S吸收較好的溶劑,因為(wei) 它價(jia) 格低廉、 反應能力強、穩定性好,且容易回收。但它存在兩(liang) 個(ge) 主要缺點,一是其蒸氣壓相當高,溶液 的損失量較大,該缺點可采用簡單的水洗方法從(cong) 氣流中吸收蒸發的胺來克服;二是它能與(yu) 氧 硫化碳COS (是裂化氣中常見的組分)反應而不能再生,所以MEA法一般隻能適合於(yu) 淨化 天然氣和其他不含COS (或CS2)的氣體(ti) 。 對含有COS的氣體(ti) ,一般使用二乙醇胺(DEA)作為(wei) 對H?S的化學吸收劑。20%〜 30%的DEA溶液可負荷0.77〜1. Omol H2S/mol胺,比MEA溶液高2-2.5倍,DEA溶液 的蒸氣壓較低,所以損失較MEA溶液要少1 /6〜1/2;所以DEA法較MEA法投資和運行 費用都低。DEA溶液對桂類溶解度較小,由該方法產(chan) 生的H?S氣體(ti) 中姪類含量V 0.5%, 便於(yu) 回收,淨化程度較高。
3.堿性鹽溶液的化學吸收法
采用堿性鹽溶液吸收H2S時,要求H2S氣體(ti) 與(yu) 吸收液反應而生成的任何化合物必須易 於(yu) 分解,以利於(yu) 吸收液的再生。一般采用強堿和弱酸的鹽類,這些鹽類使吸收液呈堿性,能 吸收酸性氣體(ti) ,而且由於(yu) 弱酸的緩衝(chong) 作用,在吸收酸性氣體(ti) 時,pH值不會(hui) 很快發生變化, 保證了係統的操作穩定性。此外堿性鹽溶液吸收H2S比吸收CO2快,當兩(liang) 種酸性氣體(ti) 同時 存在時,可以部分地選擇性吸收H2S。該類方法所用的吸收液較多,常用的主要為(wei) 碳酸鈉 溶液。碳酸鈉溶液對H2S吸收的化學反應為(wei) :
Na2 CO3 + H2S— NaHCOs+NaHS (10-9)
同時•也能吸收氣體(ti) 中的氤化氫,並且有很大一部分被吹入的空氣所氧化,其反應為(wei) :
2NaHS+2HCN+O2 —>2NaSCN+2H2O (10-10)
該方法的主要優(you) 點是設備簡單、經濟;主要缺點是一部分碳酸鈉變成了重碳酸鈉而吸收效率降低,一部分變成硫酸鹽而被消耗。用真空蒸懈再生的碳酸鈉溶液吸收H2S的方法稱 為(wei) 真空碳酸鹽法,是近年科柏公司提出的。這種改進的西柏法,可把蒸氣需求量減少至約為(wei) 常壓下的1/6,且回收的H2S濃度較高,用途較大。
4.有機溶液的物理吸收法
有機溶劑物理吸收的H2S在其分壓降低後即可解吸,克服了化學吸收法需在加熱條件 下才能解吸的不經濟缺點。大多數有機溶劑對H2S的溶解度高於(yu) 對CO2的溶解度,所以可 有選擇性地吸收H2S。該法要求H2S在氣體(ti) 中的濃度要高。當被處理氣體(ti) 的純度要求高時, 殘餘(yu) 的H2S—般采用化學吸收法再度處理。常用的物理吸收法有冷甲醇法、N-甲基-2-毗咯 烷酮法、碳酸丙烯脂法等。
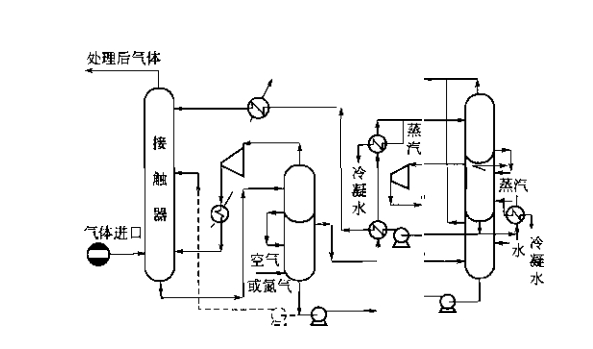
物理吸收法最簡單的流程,隻需吸收塔、常壓閃蒸罐和循環泵。典型物理吸收操作流程 見圖10-5 o
冷甲醇法采用甲醇作溶劑,在低溫(一20 75°C)和高壓(2.229MPa,即22atm) 下吸收H2S。此法主要優(you) 點是耗能少,溶液再生時因降壓被冷卻,進氣則借助高效換熱器 用淨化後的氣體(ti) 冷卻,能產(chan) 出含水極少的氣體(ti) 產(chan) 品;主要缺點是溶劑吸收重姪類,即使在低 溫下甲醇的蒸氣壓也仍然很高,蒸發損失相當大。
5.環丁硯溶液的物理化學吸收法
環丁硯的特點是兼有物理溶劑和醇胺化學吸收溶劑的特性,其物理特性來自環丁楓(二 氧四氫廛吩),而化學特性來自ADIP (二異丙醇胺)和水。在H2S氣體(ti) 分壓高的條件下, 物理環丁楓允許很高的酸性氣體(ti) 負荷,具有較大的脫硫能力;而化學溶劑ADIP可使處理過 的氣體(ti) 中殘餘(yu) H2S減少到最低值。 采用環丁楓溶劑脫硫,吸收力強、淨化率高,不僅(jin) 可脫除H2S等酸性氣體(ti) ,還可以脫 除有機硫。由於(yu) 其吸收能力強,所以溶液循環量低,溶液不易發泡,穩定性較好,使用過程 中胺變質損耗少、腐蝕性小,而且溶液加熱再生較容易,耗熱量低,特別當H2S分壓高時, 該法更為(wei) 適用。



 粵公網安備 44190002003930號
粵公網安備 44190002003930號

 掃一掃添加微信
掃一掃添加微信